- Autor Rachel Wainwright wainwright@abchealthonline.com.
- Public 2024-01-15 19:53.
- Naposledy změněno 2025-11-02 20:14.
Mnohočetný myelom
Obsah článku:
- Příčiny a rizikové faktory
-
formuláře
Rentgenové formy
- Fáze nemoci
- Příznaky myelomu
- Diagnóza mnohočetného myelomu
-
Léčba myelomu
- Antineoplastická léčba
- Podpůrná péče
- Možné komplikace a důsledky
- Předpověď
- Prevence
- Video
Mnohočetný myelom je druh rakoviny krve, maligní transformace plazmatických buněk (diferencované B-lymfocyty, podtyp leukocytů, které jsou součástí imunitního systému a syntetizují protilátky, které pomáhají tělu bojovat s infekcemi). Normálně kostní dřeň produkuje plazmatické buňky (plazmatické buňky) a B-lymfocyty v množství požadovaném tělem. V určitém okamžiku tento proces selže a místo normálních buněk se začnou vytvářet atypické (nádorové) plazmatické buňky, které postupně nahrazují normální buňky v kostní dřeni. Místo protilátek tyto buňky produkují paraproteiny, bílkoviny, které poškozují tkáň ledvin.

Myelom je charakterizován mnoha lézemi, primárně plochými kostmi, včetně kostí lebky
Mnohočetná nádorová ložiska se vyskytují v myelomu, primárně v kostní dřeni, ale také v kostech (často plochých, jako jsou lebeční kosti a žebra, ale mohou být poškozeny také tubulární kosti, zejména femur), lymfatických uzlinách a dalších orgánech. Rozmanitost lézí je způsobena jiným názvem pro myelomovou chorobu - mnohočetný myelom. Protože nádorové buňky produkují paraprotein, který chorobu označuje jako paraproteinemickou hemoblastózu, maligní imunoproliferativní onemocnění.
V zásadě jsou starší lidé - 70 let a starší náchylní k myelomu, ačkoli mladí lidé do 40 let také občas onemocní, muži jsou o něco pravděpodobnější než ženy (poměr nemocných mužů a žen je 1,4: 1). Z neznámého důvodu se toto onemocnění u lidí rasy negroidů vyskytuje dvakrát častěji než u jiných.
Synonyma: mnohočetný myelom (MM), plazmocytom, Rustitsky-Kalerova choroba (pojmenovaná podle vědců, kteří tuto chorobu poprvé popsali).
Myelomový kód podle ICD 10 - C90 (mnohočetný myelom a maligní novotvary plazmatických buněk).
Příčiny a rizikové faktory
Důvod malignity plazmatických buněk nebyl stanoven. Pravděpodobně existuje genetická predispozice. Jako mutagenní faktory mohou působit virové infekce, ionizující záření (včetně radiační terapie), karcinogeny, cytostatika (chemoterapie), chronická intoxikace. U 10% lidí s monoklonální gamopatií se transformuje na myelom.
Mezi predisponující faktory patří vše, co má potlačující účinek na imunitní systém: obezita, špatné návyky, nezdravý životní styl, nestabilita stresu atd.
formuláře
Existuje několik klasifikací MM.
Podle klinických projevů:
- symptomatický;
- asymptomatická (doutnající);
- monoklonální gamapatie neurčeného významu (MGUS).
Buněčné složení:
- flamocytární;
- plazmablastický;
- polymorfní buňka;
- malá buňka.
V závislosti na prevalenci ložisek:
- ohnisko;
- difúzní ohnisko;
- šířit.
V závislosti na typu produkovaného paraproteinu:
- G-myelom (75% všech případů);
- Myelom;
- D-myelom;
- E-myelom;
- Bence-Jonesův myelom;
- M-myelom;
- nesekretující (poslední dvě jsou vzácné formy).
S tokem:
- pomalu postupující;
- rychle postupující.
Rentgenové formy
Podle Reinberga:
- vícenásobné ohnisko;
- difúzní porotický;
- izolovaný.
Podle Lemberg:
- ohnisko;
- sukovitý;
- pletivo;
- osteolytický;
- osteoporotický;
- smíšený.
Fáze nemoci
V průběhu mnohočetného myelomu existují tři fáze:
- Počáteční.
- Rozšířený.
- Terminál.
Existuje několik kritérií pro jejich stanovení.
Mezinárodní skórovací systém (ISS) je zaměřen na množství beta-2 mikroglobulinu (β2M) a sérového albuminu:
- β2M <3,5 mg / l, albumin ≥ 3,5 g / dL.
- β2M <3,5 mg / l, albumin <3,5 g / dl; nebo β2M 3,5-5,5 mg / l, na albuminu nezáleží.
- β2M ≥ 5,5 mg / l.
Systém ISS má řadu omezení spojených se skutečností, že v některých případech se hladiny albuminu a beta-2 mikroglobulinu mohou měnit pod vlivem souběžných onemocnění, například diabetes mellitus. Proto se doporučuje korelovat tento systém stagingu s klinickou klasifikací Dury-Salmon (B. Durie, S. Salmon), podle které jsou stádia definována takto:
- Hemoglobin> 100 g / l; vápník v krvi je normou; sérový paraprotein <50 g / l pro IgG nebo <30 pro IgA; vylučování proteinu Bens-Jones (lehké řetězce imunoglobulinu) močí <4 g / den; jednoduchý plasmacytom nebo osteoporóza nebo absence obou (pro stanovení stupně I musí být splněna všechna výše uvedená kritéria).
- Kritéria nesplňují ani I., ani III.
- Hemoglobin 120 mg / l; sérový paraprotein> 70 g / l pro IgG a> 50 g / l pro IgA; vylučování Bens-Jonesova proteinu močí> 12 g / den; tři nebo více ložisek osteolýzy (ke stanovení stupně III je dostatečné dodržení pouze jednoho z uvedených kritérií).
Každá ze tří fází klasifikace Dury-Salmon je rozdělena do podskupin A a B, v závislosti na obsahu kreatininu v séru, který slouží jako indikátor funkce ledvin:
- Kreatinin <2 g / dL (<177 μmol / L).
- Kreatinin> 2 g / dl (> 177 μmol / l).
Příznaky myelomu
Než se objeví první příznaky, onemocnění postupuje asymptomaticky po dlouhou dobu (toto období může být od 5 do 15 let). V této době lze v krevním testu zjistit vysokou ROE, paraproteinemii a v moči proteinurii. Ale protože počet plazmatických buněk v kostní dřeni není zvýšen, nelze diagnózu stanovit.
Pokročilé stádium je charakterizováno výskytem a růstem příznaků, což se projevuje řadou syndromů, které mají u různých pacientů různé stupně závažnosti.
| Syndrom | Popis |
| Poškození kostí | Příznaky jsou spojeny jak s fokálním růstem nádorových plazmatických buněk ve formě kostních nádorů, tak se skutečností, že plazmatické buňky syntetizují látky, které podporují lýzu, tj. Destrukci kostní tkáně. Nejprve trpí ploché kosti (kosti pánve, lebky, lopatek, žeber, páteře), méně často - trubkovité kosti (stehenní kost, humerus). Výsledkem je intenzivní bolest v kostech, zhoršená tlakem, během pohybu se objevují patologické (nezpůsobené traumatem) zlomeniny kostí, deformity kostí. |
| Poškození hematopoetického systému | Leukopenie, trombocytopenie, plazmatické buňky v periferní krvi, zvýšené ROE, obsah myelogramu v plazmatických buňkách> 15% (u některých forem MM nemusí mít myelogram abnormality). |
| Syndrom proteinové patologie | Je to způsobeno nadprodukcí paraproteinů (patologické imunoglobuliny nebo Bens-Jonesův protein), která je doprovázena hyperproteinemií (projevující se žízní, suchou kůží a sliznicemi), proteinurií, výskytem chladných protilátek (projevující se alergií na chlad, akrocyanózou, trofickými poruchami končetin), amyloidem části těla, kde došlo k usazování amyloidu, zvětšení rtů a jazyka). |
| Myelomová nefropatie | Pozoruje se u 80% pacientů s MM, charakterizovaných rozvojem chronického selhání ledvin, které se projevuje slabostí, nevolností, sníženou chutí k jídlu a úbytkem hmotnosti. Edém, ascites, hypertenze (jeden z diagnostických příznaků) nejsou charakteristické. |
| Viscerální syndrom | V důsledku infiltrace nádorových plazmatických buněk se ve všech vnitřních orgánech vyvíjejí léze jater, sleziny (častěji), gastrointestinálního traktu, pleury (méně často) s vývojem charakteristických příznaků. |
| Sekundární imunodeficience | Náchylnost k infekcím, běžná respirační virová onemocnění jsou závažná, často komplikovaná přidáním bakteriální infekce, infekční a zánětlivá onemocnění močových cest, pásový opar, plísňové infekce nejsou neobvyklé. |
| Zvýšená viskozita krve | Je charakterizována zhoršenou mikrocirkulací, která se projevuje zrakovým postižením, svalovou slabostí, bolestmi hlavy, rozvojem trofických kožních lézí, trombózou. Je pozorován u 10% pacientů s MM. |
| Hemoragický syndrom | Vyvíjí se v důsledku snížení funkčnosti krevních destiček a aktivity faktorů srážení krve. Projevuje se krvácením dásní, krvácením z nosu, vícečetnými hematomy. |
| Neurologický syndrom | Je to způsobeno infiltrací dura mater plazmatickými buňkami, deformací kostí lebky a obratlů, kompresí nervových kmenů nádory. Projevuje se jako periferní neuropatie, svalová slabost, zhoršení všech typů citlivosti, parestézie, snížení šlachových reflexů a další příznaky v závislosti na oblasti léze. |
| Hyperkalcémie | Je to způsobeno vyluhováním vápníku z kostní tkáně v důsledku lýzy. Projevuje se nevolností, zvracením, ospalostí, poruchami vědomí, ztrátou orientace. |
Konečné stádium je charakterizováno exacerbací stávajících příznaků, rychlou destrukcí kostí, množením nádorů do sousedních tkání, zvyšujícím se selháním ledvin, těžkou anémií a infekčními komplikacemi.
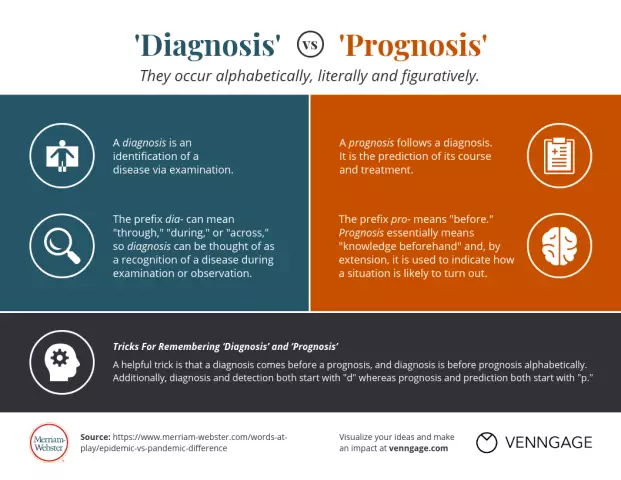
Diagnóza mnohočetného myelomu
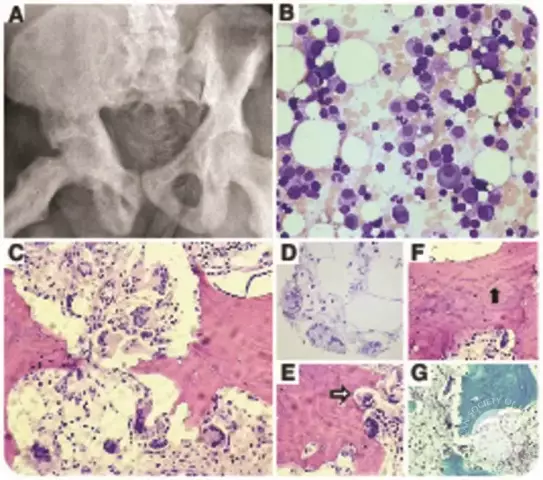
Hlavními příznaky mnohočetného myelomu jsou plazmacytóza kostní dřeně (> 10%), ložiska osteolýzy, M-gradient (monoklonální protein) nebo Bence-Jonesův protein v séru nebo moči. Právě na těchto známkách se provádí diagnostické vyhledávání s podezřením na onemocnění a pro diagnózu postačuje stanovení plasmacytózy a M-gradientu (nebo proteinu Bens-Jones) bez ohledu na přítomnost kostních změn.

U mnohočetného myelomu se v kostní dřeni nachází nadměrné množství plazmatických buněk
Používají se následující diagnostické metody:
- RTG lebky, hrudníku, pánve, páteře, ramenního pletence, pažní kosti a stehenní kosti.
- Spirální počítačová tomografie.
- Magnetická rezonance.
- Pozitronová emisní tomografie.
- Aspirační biopsie kostní dřeně k určení myelogramu.
- Laboratorní analýzy krve a moči.
- Cytogenetický výzkum.
Kostní a extraoseální léze u mnohočetného myelomu jsou zkráceny jako CRAB:
- C - vápník (vápník) - hyperkalcémie, obsah Ca> 2,75;
- R - Renální (renální) - porucha funkce ledvin, kreatinin v séru> 2 mg / dl;
- A - Anémie (anémie) - normocytová a normochromní, hemoglobin <100 g / l;
- В - Kost (kost) - ložiska osteolýzy, patologické zlomeniny, osteopenie atd.
Diferenciální diagnostika se provádí s následujícími patologiemi:
- další monoklonální gamapatie;
- polyklonální hypergamaglobulinemie;
- reaktivní polyklonální plazmacytóza;
- kostní metastázy.
Léčba myelomu
Mnohočetný myelom je nevyléčitelný, avšak adekvátní léčba vám umožní dosáhnout stabilní remise a udržet ji po dlouhou dobu.
Terapie se provádí ve dvou směrech: protinádorový (etiotropický) a podpůrný (symptomatický).
Antineoplastická léčba
Předepisuje se s ohledem na věk pacienta a přítomnost doprovodných onemocnění. Pacientům do 70 let nebo nad 70 let bez doprovodné patologie jsou předepsány 4-6 cyklů polychemoterapie s následnou mobilizací hematopoetických buněk, následnou vysokodávkovou chemoterapií (myeloablace) a následnou podporou autologní transplantace kmenových buněk. V budoucnu, po 3-4 měsících, se uvažuje o výhodnosti několika dalších kurzů polychemoterapie nebo jiné autotransplantace kmenových buněk.
Pacientům s kontraindikacemi k takové léčbě (pacienti starší 70 let se současnou patologií) je předepsána polychemoterapie.
Podpůrná péče
Provádí se v následujících oblastech:
- léčení renální dysfunkce;
- potlačení osteolýzy;
- odstranění hyperkalcémie;
- léčba syndromu vysoké viskozity krve;
- léčba anémie;
- úleva od syndromu bolesti;
- antitrombotická terapie;
- prevence infekce.
U asymptomatické formy mnohočetného myelomu není léčba nutná; lékařský dohled je dostatečný.
Možné komplikace a důsledky
Mnohočetný myelom se může transformovat na akutní plazmablastickou leukémii nebo lymfosarkom.
Předpověď
V závislosti na formě myelomu a citlivosti na léčbu lze 5letého přežití dosáhnout u 40-80% pacientů. Mezi nepříznivé prognostické faktory patří relapsy; po každém relapsu je obtížnější dosáhnout remise. Smrt ve většině případů nastává v důsledku závažných infekčních komplikací.
Prevence
Prevence mnohočetného myelomu spočívá v vyhýbání se kontaktu s karcinogeny a toxickými látkami a v udržování zdravého životního stylu.
Video
Nabízíme k prohlížení videa na téma článku.

Anna Kozlová Lékařská novinářka O autorce
Vzdělání: Rostovská státní lékařská univerzita, obor „Všeobecné lékařství“.
Informace jsou zobecněny a poskytovány pouze pro informační účely. Při prvních známkách nemoci navštivte svého lékaře. Samoléčba je zdraví škodlivá!